Alumnos finalizó el trimestre, ¡¡¡excelentes los exámenes !!! nos encontraremos nuevamente luego de las vacaciones de invierno, para continuar aprendiendo cada ves más sobre el mundo de la Química. ¡Éxitos!
QUÍMICA BÁSICA
"Enseñar no es transferir conocimiento, sino crear las posibilidades para su construcción. Quien enseña aprende al enseñar y quien enseña aprende a aprender"... Paulo Freire
domingo, 15 de junio de 2014
miércoles, 11 de junio de 2014
9- Soluciones ácidas, básicas y neutras. pH
Hola alumnos en base a lo desarrollado en la clase de hoy, les dejo esta presentación, con el fin de que les sea de ayuda y de apoyo para una mejor comprensión. Hecho ésto, doy por finalizado, el contenido.
lunes, 9 de junio de 2014
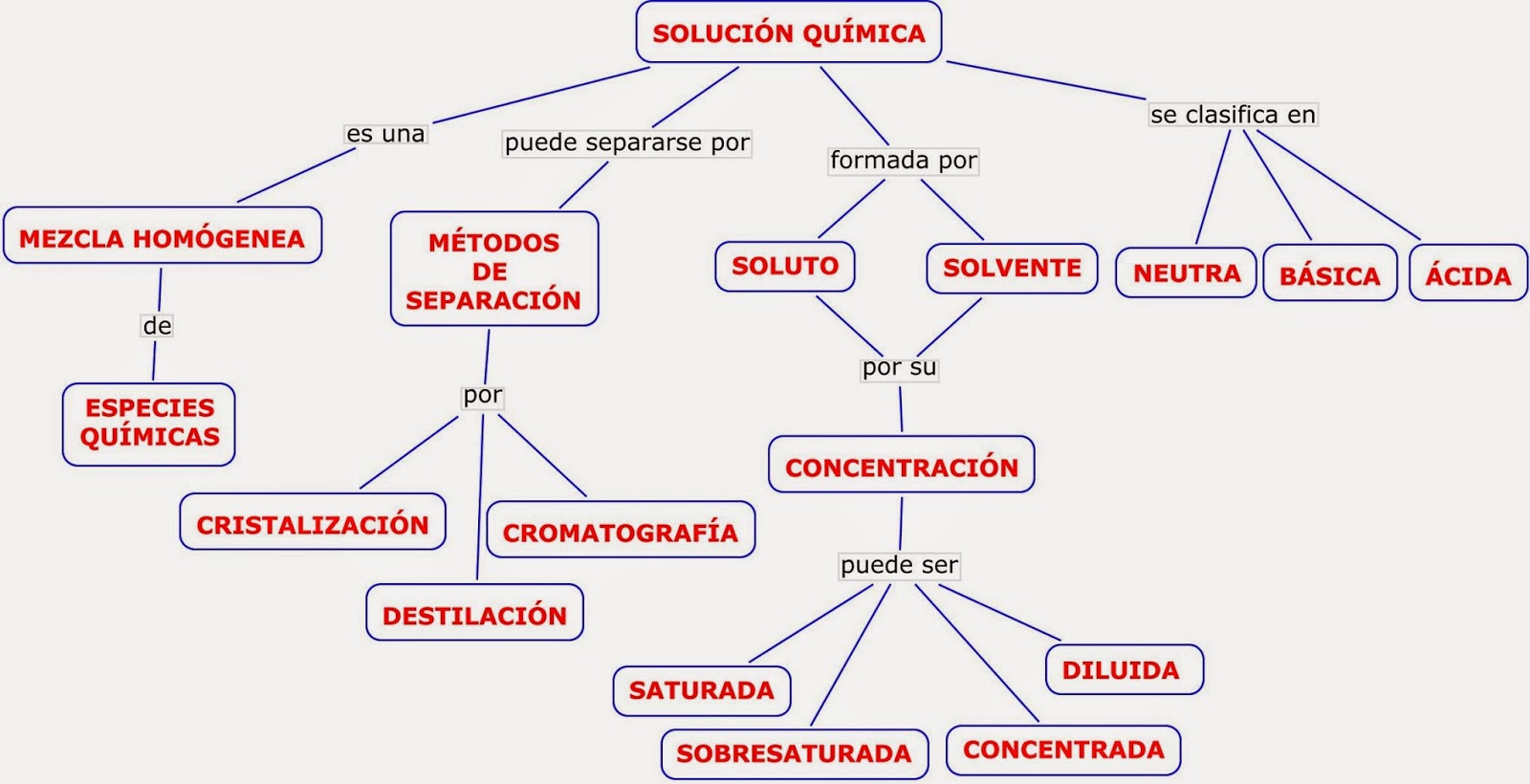
8-Mapa conceptual
Hola alumnos!!!! este mapa conceptual le será de gran utilidad a la hora de estudiar para la evaluación del tema soluciones. deberán tenerlo en sus carpetas ya sea impreso o mano escrito. saludos
viernes, 6 de junio de 2014
Método de separación
Alumnos les dejo este link, donde encontrarán el apunte de métodos de separación de soluciones, deberán tenerlo mano escrito o impreso en sus carpetas para la próxima clase. ¡Saludos!
miércoles, 4 de junio de 2014
6-Concentración de soluciones
CONCENTRACIÓN DE SOLUCIONES
Hola alumnos en este link podrán encontrar los apuntes del tema Concentración de Soluciones que desarrollaremos en la próxima clase!!!miércoles, 28 de mayo de 2014
Sistemas homogéneos
Hola alumnos les propongo ver el siguiente vídeo!!!!!!
- Sistemas homogéneos y sustancias puras naturales!!!!
- En base al vídeo y a lo desarrollado, realizar la siguiente ACTIVIDAD !!! que será controlada la próxima clase.
lunes, 26 de mayo de 2014
CONCENTRACIÓN
CONCENTRACIÓN
Hola alumnos!!! hoy desarrollaremos "tipos de concentraciones de una solución".
Ya hemos visto que las disoluciones son mezclas de dos o más sustancias, por lo tanto se pueden mezclar agregando distintas cantidades: Para saber exactamente la cantidad de soluto y de solvente de una disolución se utiliza una magnitud denominada concentración.
Dependiendo de su concentración las disoluciones se clasifican en diluidas, concentradas, saturadas, sobresaturadas.
- Diluidas: si la cantidad de soluto respecto del solvente es pequeña. Ejemplo: una solución de 1 gramo de sal de mesa en 100 gramos de agua.
- Concentradas: si la proporción de soluto con respecto del solvente es grande. Ejemplo: una disolución de 25 gramos de sal de mesa en 100 gramos de agua.
- Saturadas: se dice que una disolución está saturada a una determinada temperatura cuando no admite más cantidad de soluto disuelto. Ejemplo: 36 gramos de sal de mesa en 100 gramos de agua a 20º C.
- Sobresaturadas: disolución que contiene mayor cantidad de soluto que la permitida a una temperatura determinada. La sobresaturación se produce por enfriamientos rápidos o por descompresiones bruscas. Ejemplo: al sacar el corcho a una botella de refresco gaseoso.
- Ejemplo
Suscribirse a:
Entradas (Atom)